Tulisan (Softskill)
Teori ATOM Menurut Niels Bohn
Teori atom Niels Bohr
Pak Niels Bohr mengenalkan teori tentang lintasan-lintasan electron
Ternyata
benar segala sesuatu yang ada di dunia ini tidak ada yang sempurna.
Setiap teori yang dikeluarkan ilmuwan pasti disamping ada kelebihannya,
juga ada kekurangannya. Dengan percobaannya, tahin 1911, Niels Bohr
berusaha memperbaiki teori Rutherford dengan melakukan percobaan
spectrum atom hydrogen.
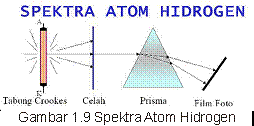
Lalu dari percobaan tersebut, gimana si teori atom Pak Niehl Bohr ni?
1. Menurutnya, Hanya ada seperangkat orbit tertentu yang diperbolehkan bagi satu elektron dalam atom hidrogen. Orbit ini dikenal sebagai keadaan gerak stasioner (menetap) elektron dan merupakan lintasan melingkar disekeliling inti
- Selama elektron berada dalam lintasan stasioner, energi elektron tetap sehingga tidak ada energi dalam bentuk radiasi yang dipancarkan maupun diserap.
- Elektron hanya dapat berpindah dari satu lintasan stasioner ke lintasan stasioner lain. Pada peralihan ini, sejumlah energi tertentu terlibat, besarnya sesuai dengan persamaan planck, ΔE = hv.
- Lintasan stasioner yang dibolehkan memilki besaran dengan sifat-sifat tertentu, terutama sifat yang disebut momentum sudut. Besarnya momentum sudut merupakan kelipatan dari h/2∏ atau nh/2∏, dengan n adalah bilangan bulat dan h tetapan planck
Jadi
menurut pak bohr, electron-elektron mengelilingi inti pada
lintasan-lintasan tertentu yang disebut kulit electron atau tingkat
energi.tingkat energy paling rendah adalah kulit electron yang terletak
paling dalam.semakin keluar semakin besar nomor kulitnya dan semakin
tinggi tingkat energinya.


Kelebihan
atom Bohr adalah bahwa atom terdiri dari beberapa kulit untuk tempat berpindahnya elektron.
Kelemahan
model atom ini adalah tidak dapat menjelaskan efek Zeeman dan efek Strack
atom Bohr adalah bahwa atom terdiri dari beberapa kulit untuk tempat berpindahnya elektron.
Kelemahan
model atom ini adalah tidak dapat menjelaskan efek Zeeman dan efek Strack
Tidak ada komentar:
Posting Komentar